Kritische Temperatur
[711] Kritische Temperatur. Cagniard de la Tour [1], Drion, Andrews u.a. beobachteten, daß bei genügender Erwärmung einer Flüssigkeit eine Temperatur[711] erreicht werde, für welche die vorher sichtbar gewesene scharfe Grenze zwischen; Flüssigkeit und Dampf verschwand und der ganze Raum von einer homogenen Masse erfüllt schien. Man schloß hieraus, daß oberhalb jener sogenannten kritischen Temperatur der Körper nicht mehr als Flüssigkeit bestehen könne, wie sehr auch der Druck erhöht werden möge, oder daß doch der Unterschied zwischen dem flüssigen und dem gasförmigen Zustand oberhalb der kritischen Temperatur hinfällig sei.
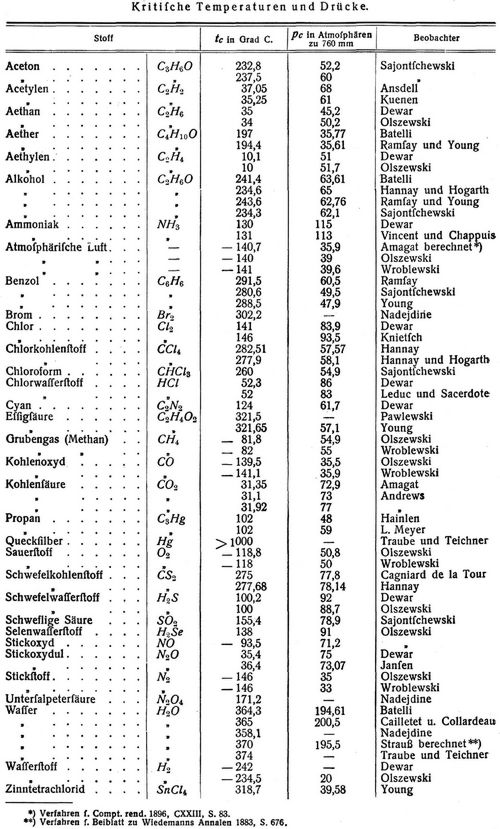
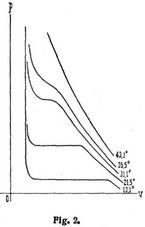
Wird anfänglich überhitzter Dampf (s. Dampf und Dampf, überhitzter) bei irgend einer konstanten Temperatur t komprimiert, so geht er unter gewöhnlichen Verhältnissen zuerst in den gesättigten Zustand und dann nach und nach in Flüssigkeit über. Die Druckkurve p = f (v) (s. Aeußere Arbeit) würde hierbei nacheinander das Gesetz der isothermischen Zustandsänderung überhitzten Dampfes, nassen Dampfes und reiner Flüssigkeit befolgen. In Fig. 1 möge dieselbe durch die fettere Linie angedeutet sein, während G die Grenzkurve des reinen Dampfes und F die Zustandskurve der reinen Flüssigkeit für den Siedepunkt bezeichnen (vgl. Dampf), so daß den auf einer Horizontalen p liegenden Punkten von F und G die spezifischen Volumen σ, s der reinen Flüssigkeit im Siedepunkt t = f (p) und des reinen gesättigten Dampfes von der gleichen Temperatur entsprechen. Der hier angenommene Verlauf der Isothermen wurde durch Versuche von Andrews [3] mit Kohlensäure von t = 13,1° und 21,5° so weit bestätigt (Fig. 2) als bei der nicht vollkommenen Reinheit der Kohlensäure zu erwarten war. Dagegen zeigte sich, daß von einer gewissen Temperatur an nichts mehr von dem horizontalen Kurvenstück übrigblieb und auch keine Verflüssigung zu bemerken war. Diese Temperatur wäre also die kritische Temperatur tc gewesen; für die Kohlensäure betrug sie etwa tc = 31,1°. Druck und Volumen für den Berührungspunkt der Isotherme te mit der Grenzkurve FG (Fig. 1) werden kritischer Druck pc und kritisches Volumen vc genannt, wonach pc den höchstmöglichen Druck gesättigten Dampfes im gewöhnlichen Sinne bedeutet, da oberhalb FG keine Verflüssigung mehr eintreten soll. Der Zustand pc, vc, tc wird häufig als kritischer Zustand bezeichnet. In der Tabelle S. 713 sind die durch Versuche ermittelten tc, pc für eine Anzahl Körper angeführt; weitere Resultate s. [15] und [23], S. 860; betreffend Gemische vgl. [23], S. 850.
Die kritischen Werte (kritischen Daten) tc, vc, pc lassen sich auch berechnen. Die allgemeinen Beziehungen zwischen p, v, t (Zustandsgleichungen), welche van der Waals, Clausius, Sarrau u.a. mit besonderer Rücksicht auf das Verhalten der Kohlensäure aufgestellt haben (s. Bd. 4, S. 277) gelten sowohl für reinen Dampf als für reine Flüssigkeit, sie setzen nur die Homogenität der ganzen Masse voraus. Diese ist nun zwischen F und G nicht vorhanden, da wir hier ein Gemisch von Flüssigkeit und Dampf haben. Verzeichnen wir gleichwohl die Isotherme t entsprechend jenen Gleichungen auch durch dieses Gebiet, so ergibt sich ein Verlauf ähnlich dem in Fig. 1 punktiert angedeuteten. Derselbe würde also für den Fall gelten, daß der Dampf ohne Verletzung der Homogenität oder, wie man sich ausdrückt, auf kontinuierliche Weise in Flüssigkeit übergeführt werden könnte. Die wirkliche Isotherme wird von der hypothetischen dreimal geschnitten, entsprechend den drei Wurzeln v, welche jene Gleichungen drittem Grades für ein bestimmtes p besitzen (Fig. 1). Die hypothetische Isotherme zeigt ein Minimum, einen Wendepunkt und ein Maximum. Jene drei Wurzeln wie diese drei Punkte nähern sich mit wachsender Temperatur immer mehr und fallen beim Verschwinden des horizontalen Stücks der wirklichen Isotherme, d.h. für den kritischen Zustand pc, vc, tc zusammen. Oberhalb der kritischen Temperatur sind alle drei Wurzeln v der erwähnten Zustandsgleichungen imaginär.
Nach dem Gesagten besitzen wir zwei Mittel, die kritischen Größen pc, vc, tc zu berechnen, indem wir neben der Zustandsgleichung entweder die zwei Gleichungen verwenden können, welche durch Gleichsetzen der drei Wurzeln der Zustandsgleichung entstehen, oder aber die zwei Gleichungen, welche die auf die Zustandsgleichung angewendeten Bedingungen dp/dv = 0 und d2p/dv2 = 0 ergeben. Den ersten Weg hat zuerst van der Waals eingeschlagen ([5], S. 92), der zweite wurde zuerst von Sarrau gewählt [8], S. 944. Mit den Bd. 4, S. 277, erwähnten Bezeichnungen erhält man nach der Zustandsgleichung von van der Waals:
nach der ersten Zustandsgleichung von Clausius:
nach der Zustandsgleichung von Sarrau:
Diese Gleichungen ergeben bei geeigneter Wahl der Konstanten genügende Uebereinstimmung mit Versuchsresultaten.[712]
[713] Um die Verdampfung einer Flüssigkeit bei einem bestimmten Drucke p zu bewirken, muß, abgesehen von der Ueberwindung des äußeren Drucks, eine gewisse Wärmemenge, die innere Verdampfungswärme ρ, aufgewendet werden (s. Dampf, gesättigter, Verdampfungswärme), welche zur Ueberwindung innerer Widerstände dienen soll. Da jedoch bei Ueberschreiten der kritischen Temperatur die Verdampfung ohne äußere Arbeit (bei konstantem Volumen) von selbst vor sich geht, so schloß zuerst Mendelejeff [2], daß
für t = tc, ρ = Au (T dp/dt – p) = 0
4.
(u = s – σ, vgl. Clapeyronsche Gleichung). Aus dem gleichen Grunde wurde tc mitunter nach Mendelejeff die absolute Siedetemperatur genannt (vgl. Dampf). Läßt sich nun beispielsweise ausdrücken ρ = α – ß t mit von t unabhängigen α, ß, so folgt tc = α : ß. Die von Zeuner auf Grund Regnaultscher Versuchsresultate aufgestellten Gleichungen jener Form (s. Verdampfungswärme) liefern zwar von den beobachteten tc stark abweichende Werte, allein die Versuche blieben weit unter der kritischen Temperatur und Avenarius konnte die Konstanten a, ß, entsprechend den Ergebnissen Regnaults, auch so wählen, daß genügende Uebereinstimmung der beobachteten und aus tc = α : ß berechneten tc entstand [4]. Mathias erhielt bei Versuchen mit Kohlensäure bis nahe der kritischen Temperatur (bis 30,82°) Werte von ρ, welche für tc auf ρ = 0 schließen ließen [10].
Ramsay [6], Jamin [7] und Lippmann [11] definierten die kritische Temperatur lediglich als diejenige Temperatur, bei welcher die Flüssigkeit und ihr gesättigter Dampf gleiche Dichten, d.h. auch gleiche spezifische Volumen σ, s erlangen, wonach wegen u = s – σ = 0 Bedingung 4. und die Schlüsse auf Grund von Fig. 1 bestehen bleiben. Andre von den vorgetragenen abweichenden Ansichten über die kritische Temperatur haben vorläufig wenig Anklang gefunden, wozu erheblich beitrug, daß die Beobachtungsresultate durch die obenerwähnten Zustandsgleichungen eine gewisse Bestätigung erhielten. Ramsay hat seine Einwände später zurückgezogen. Immerhin sind bezüglich des Wesens der kritischen Temperatur noch keineswegs alle Zweifel gehoben. Vgl. z.B. [20], [23], S. 837.
Nach dem dargelegten Begriffe der kritischen Temperatur besteht eine Kontinuität des gasförmigen und flüssigen Zustandes derart, daß man einen Körper aus dem einen in den andern überführen kann, ohne jemals die Homogenität der ganzen Masse aufzugeben, ohne jemals ein Gemisch von Dampf und Flüssigkeit verschiedener Dichten zu erhalten. Man muß nur den richtigen Weg einschlagen. Bleiben wir immer unter der kritischen Temperatur, so läßt sich die Flüssigkeit nur so in die Gasform überführen, daß wir zeitweise ein nicht homogenes Gemenge von Dampf und Flüssigkeit vor uns haben (zwischen F und G in Fig. 1). Bringen wir jedoch die Flüssigkeit zunächst ohne Verdampfung, z.B. in einem vollständig ausgefüllten Räume, über die kritische Temperatur, so kann sie auch in jeden andern Zustand reinen Dampfes übergeführt werden (außerhalb FG in Fig. 1), ohne daß von Anfang an jemals die Homogenität verletzt würde. Es hat deshalb schon Andrews den flüssigen und gasförmigen Zustand als weit auseinander gelegene Fälle ein und derselben Aggregatform angesehen [3], eine Auffassung, welche besonders durch van der Waals weiter verfolgt worden ist [5].
Literatur: [1] Cagniard de la Tour, Exposé de quelques résultats obtenus par l'action combinée de la chaleur et de la compression sur certains liquides, Annales de chimie et de physique 1822, XXI, S. 127, 178; 1823, XXII, S. 410. – [2] Mendelejeff, Ueber die Ausdehnung der Flüssigkeiten beim Erwärmen über ihren Siedepunkt, Annalen der Chemie und Pharmacie 1861, CXIX, S. 11 (vgl. Poggendorffs Ann. 1870, CXLI, S. 618). – [3] Andrews, On the continuity of the gaseous and liquid states of matter, Philosophical Transactions 1869, II, S. 575 (Poggendorffs Ann. 1871, Ergänzungsband V, S. 64). – [4] Avenarius, Ueber die innere latente Wärme, Poggendorffs Ann. 1874, CLI, S. 303. – [5] Van der Waals, Die Kontinuität des gasförmigen und flüssigen Zustandes, deutsch von Roth, Leipzig 1881, S. 168. – [6] Ramsay, On the critical point of the liquefiable gases, Philosophical Magazine 1883, XVI, S. 118 (vgl. bezüglich der Einwände gegen Andrews Auffassung 1894, XXXVII, S. 215). – [7] Jamin, Sur le point critique des gaz liquéfiables, Comptes rendus 1883, XCVI, S. 1448 (s.a. 1883, XCVII, S. 10). – [8] Sarrau, Sur la compressibilité des fluides, Comptes rendus 1885, Cl, S. 941, 994. – [9] Wroblewski, Wiener Berichte 1885, XCI, S. 696; 1885, XCII, S. 641; 1888, XCVII, S. 1359. – [10] Mathias, Sur la chaleur de vaporisation de l'acide carbonique au voisinage du point critique, Comptes rendus 1889, CIX, S. 470. – [11] Lippmann, Cours de thermodynamique, Paris 1889, S. 177. – [12] Cailletet et Collardeau, Recherches sur la tension de la vapeur saturée jusqu'au point critique, Journal de physique 1891, X, S. 333 (Wasser). – [13] Gouy, Effets de la pesanteur sur les fluides an point critique, Comptes rendus 1892, CXV, S. 720. – [14] Galitzine, Ueber den Zustand der Materie in der Nähe des kritischen Punktes, Wiedemanns Annalen 1893, L, S. 521. – [15] Landolt und Börnstein, Physikalisch-chemische Tabellen, Berlin 1894, S. 84. – [16] Olszewski, On the liquefaction of gases, Philosophical Magazine 1895, XXXIX, S. 188 (Tabelle S. 210, Aufsätze von Olszewski, S. 211). – [17] Ders., Bestimmung der kritischen und der Siedetemperatur des Wasserstoffs, Wiedemanns Annalen 1895, LVI, S. 133. – [18] Dieterici, Ueber den kritischen Zustand, Wiedemanns Annalen 1899, LXIX, S. 685. – [19] Zeuner, Technische Thermodynamik, II, Leipzig 1901, S. 187,193. – [20] Traube, Theorie der kritischen Erscheinungen und der Verdampfung, Annalen der Physik 1902, VIII, S. 267. – [21] Schäfer, Die kritischen Daten und ihre Bedeutung für die Kondensation der Gase, Zeitschr. d. Ver. deutsch. Ing. 1902, S. 1902. – [22] Mathias, Le point critique des corps purs, Paris 1904. – [23] Winkelmann, Handbuch der Physik, III, Wärme, Leipzig 1906, S. 830. – [24] Weyrauch, Grundriß der Wärmetheorie, II, Stuttgart 1907, S. 77.
Weyrauch.
Brockhaus-1809: Die Temperatur · die kritische Philosophie
Eisler-1904: Kritische Metaphysik
Lueger-1904: Temperatur [2] · Temperatur [3] · Temperatur [1] · Schmelzpunkt, -temperatur, -wärme · Kritische Daten, Kritischer Druck, Kritischer Zustand, Kritisches Volumen
Meyers-1905: Potentĭelle Temperatur · Temperatūr · Kritische Geschwindigkeit · Kritische Tage · Kritische Zeit
Pierer-1857: Mittlere Temperatur · Temperatur · Kritische Tage
Buchempfehlung
Hume, David
Dialoge über die natürliche Religion
Demea, ein orthodox Gläubiger, der Skeptiker Philo und der Deist Cleanthes diskutieren den physiko-teleologischen Gottesbeweis, also die Frage, ob aus der Existenz von Ordnung und Zweck in der Welt auf einen intelligenten Schöpfer oder Baumeister zu schließen ist.
88 Seiten, 4.80 Euro
Im Buch blättern
Ansehen bei Amazon
Buchempfehlung
Geschichten aus dem Biedermeier. Neun Erzählungen
Biedermeier - das klingt in heutigen Ohren nach langweiligem Spießertum, nach geschmacklosen rosa Teetässchen in Wohnzimmern, die aussehen wie Puppenstuben und in denen es irgendwie nach »Omma« riecht. Zu Recht. Aber nicht nur. Biedermeier ist auch die Zeit einer zarten Literatur der Flucht ins Idyll, des Rückzuges ins private Glück und der Tugenden. Die Menschen im Europa nach Napoleon hatten die Nase voll von großen neuen Ideen, das aufstrebende Bürgertum forderte und entwickelte eine eigene Kunst und Kultur für sich, die unabhängig von feudaler Großmannssucht bestehen sollte. Dass das gelungen ist, zeigt Michael Holzingers Auswahl von neun Meistererzählungen aus der sogenannten Biedermeierzeit.
- Georg Büchner Lenz
- Karl Gutzkow Wally, die Zweiflerin
- Annette von Droste-Hülshoff Die Judenbuche
- Friedrich Hebbel Matteo
- Jeremias Gotthelf Elsi, die seltsame Magd
- Georg Weerth Fragment eines Romans
- Franz Grillparzer Der arme Spielmann
- Eduard Mörike Mozart auf der Reise nach Prag
- Berthold Auerbach Der Viereckig oder die amerikanische Kiste
434 Seiten, 19.80 Euro
Ansehen bei Amazon
- ZenoServer 4.030.014
- Nutzungsbedingungen
- Datenschutzerklärung
- Impressum