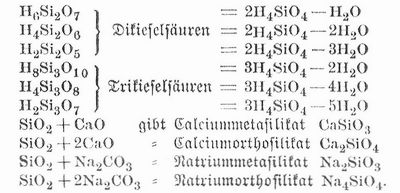Kieselsäuresalze
[896] Kieselsäuresalze (Silikate) finden sich weitverbreitet im Mineralreich und entstehen bei Einwirkung von Kieselsäure auf die Basen, auch beim Erhitzen von Kieselsäure mit den Salzen der weniger feuerbeständigen Säuren, die unlöslichen auch durch Wechselzersetzung. In Wasser löslich sind nur die K. der Alkalimetalle, alle K. sind schmelzbar, einige aber nur bei sehr hoher Temperatur; sie erstarren kristallinisch oder glasig, und besonders die Doppelsilikate geben ausgezeichnete Gläser (Glas, Schlacke). Aus den löslichen wird die Kieselsäure durch stärkere Säuren als Gallerte abgeschieden; die unlöslichen werden zum Teil durch Kochen mit Säuren unter Abscheidung von Kieselsäure aufgeschlossen, andre werden nur durch Schmelzen mit kohlensauren Alkalien zersetzt. Mit Flußspat und Schwefelsäure erwärmt oder mit Flußsäuredämpfen behandelt, entwickeln alle K. Kieselfluorid. Die durch Salzsäure aufschließbaren wasserhaltigen K. (Zeolithe) verlieren beim Erhitzen das Wasser und die Zersetzbarkeit durch Säuren, während manche andre wasserhaltige Silikate nach dem Glühen durch Säuren leichter zersetzbar sind als vorher. Im allgemeinen werden die K. um so leichter zersetzt, je mehr die Basis in ihnen vorwaltet, und je mehr Wasser sie enthalten. Man unterscheidet Orthosilikate, die der Orthokieselsäure H4SiO4 entsprechen, z. B. Olivin Mg2SiO4, Zirkon Zr Si O4, und Metasilikate, die sich von der Metakieselsäure H2SiO3 ableiten, wie Wollastonit CaSiO3, Enstatit MgSiO3 u. a. Die in der Natur vorkommenden Silikate (s. d.) stehen zum bei weitem größten Teil in Beziehung zu anhydrischen Säuren, die aus zwei oder mehreren Molekülen Orthokieselsäure durch Austritt von Wasser entstanden sind und der allgemeinen Formel xH4SiO4-yH2O entsprechen (Polykieselsäuren). Je nach der Anzahl der in dem Molekül der anhydrischen Kieselsäure enthaltenen Siliciumatome unterscheidet man Di-, Tri-, Tetrakieselsäuren und dem entsprechende Di-, Tri- und Tetrasilikate nach den Formeln:
Zwischen diesen Grenzen schmelzen basische Oxyde mit den Silikaten zu einer gleichförmigen Schmelze zusammen, zu einem Gemenge von komplexen Polysilikaten, das wenig Neigung zur Kristallisation besitzt und beim Erstarren ein durchsichtiges Glas liefert. K. finden mannigfache Verwendung, die der Alkalien als Wasserglas, die der Tonerde in den Tonwaren und, wie die übrigen, besonders in Doppelsilikaten, als welche sie das Glas, die Schlacken bilden und in den Zementen eine große Rolle spielen.
- ZenoServer 4.030.014
- Nutzungsbedingungen
- Datenschutzerklärung
- Impressum