Silber
[463] Silber (Argentum, hierzu Tafel »Silbergewinnung« mit Text) Ag, Metall, findet sich gediegen, in regulären Kristallen, drahtförmig, moosartig, gestrickt (s. Tafel »Mineralien und Gesteine«, Fig. 8), in Platten, derb und eingesprengt, oft gold-, kupfer-, antimon-, arsen-, eisenhaltig, auf Erzgängen, besonders in Gesellschaft von Silbererzen mit Bleiglanz und Kalkspat, im Erzgebirge und Harz, im Schwarzwald, bei Schemnitz, bei Kongsberg, in Spanien, am Altai, in Mexiko, Chile, Peru, Kalifornien und am Obern See, auch mit Quecksilber legiert als Amalgam, mit Antimon als Antimonsilber, mit Tellur als Tellursilber, mit Schwefel verbunden als Silberglanz Ag2S mit 87 Proz. S., mit Antimon und Schwefel als dunkles Rotgiltigerz Ag3SbS3 mit 59,8 Proz. S., Sprödglaserz Ag5SbS4 mit 68,4 Proz. S. und als Silberantimonglanz AgSbS2 mit 36,75 Proz. S., mit Arsen und Schwefel verbunden als lichtes Rotgiltigerz Ag3AsS3 mit 65,5 Proz. S., mit Kupfer, Antimon, Arsen und Schwefel verbunden als Polybasit 9(Ag2Cu2)S + Sb2As2S3 mit 64–72 Proz. S., mit Kupfer und Schwefel als Kupfersilberglanz, mit Chlor verbunden als Hornsilber, auch mit Brom und Jod verbunden etc. Silbererze mit erdigen Substanzen, auch andern geschwefelten Erzen gemengt, bilden die Dürrerze. Außerdem tritt S. in Erzen andrer Metalle auf, von denen die oxydierten silberärmer zu sein pflegen als die geschwefelten; von letztern sind am ärmsten die eisenhaltigen (Schwefel- und Magnetkies), dann folgen die zinkischen (Zinkblende), die kupferhaltigen (Kupferglanz, Buntkupfererz, Kupferkies, Fahlerze) und die bleihaltigen (Bleiglanz). Bei Fahlerzen steigt der Silbergehalt zuweilen so hoch (bis 30 Proz. und mehr), daß sie zu den Silbererzen zu rechnen sind. Aller Bleiglanz enthält wenigstens Spuren von S., am gewöhnlichsten 0,01–0,03, zuweilen bis 0,5 Proz., selten über 1 Proz., als isomorphes Schwefelsilber; größere Silbergehalte deuten meist auf eine Einsprengung von eigentlichen Silbererzen in den Bleiglanz. Arsen- und Antimonerze sind meist silberarm, wenn nicht Silbererze beigemengt sind; Wismut-, Nickel- und Kobalterze besitzen oft einen gewinnungswürdigen Silbergehalt. Über die Gewinnung s. beifolgende Tafel mit Tert.
Reines S. erhält man durch Schmelzen von Chlorsilber mit kohlensaurem Alkali oder durch Übergießen von Chlorsilber mit verdünnter Salzsäure und Reduktion mit Zink oder Eisen. In der Technik löst man käufliches S. in konzentrierter Schwefelsäure und das erhaltene Sulfat in viel warmem Wasser, wobei die Edelmetalle zurückbleiben. Dann fällt man das S. durch Eisen und schmilzt es. Bei der elektrolytischen Scheidung hängt man das S. als Anode in eine salpetersaure Silbernitratlösung und sammelt das an der aus Silberblech bestehenden Kathode sich kristallinisch ausscheidende S. Mit der Knallgasflamme kann man S. destillieren. In sein verteilter (molekularer) und daher reaktionsfähiger Form erhält man S. durch Reduktion von frisch gefälltem Chlorsilber mit Formaldehydlösung und Kaliumkarbonat oder mit Natronlauge und Traubenzucker oder auf elektrolytischem Wege. Erhitzt man zitronensaures S. im Wasserstoffstrom auf 100°, so bleibt ein wesentlich aus S. bestehender Rückstand, der mit Wasser eine intensiv gefärbte Lösung gibt, die durch Dialyse gereinigt werden kann (kolloidales S.) und am haltbarsten ist, wenn sie noch andre Kolloidsubstanzen enthält. Silbernitrat mit Formaldehyd und Wasserglas gibt braune bis grüne Lösungen, Silbernitrat mit arabischem Gummi und Hydrazinhydrat gibt eine rote, im reflektierten Licht olivengrüne Lösung. Aus den Lösungen (Hydrosole) fällen Glaubersalz, Salpeter und andre Salze festes kolloidales S.-Reines S. ist weiß, in sehr dünner Schicht blau durchscheinend, gut polierbar, auf dem Bruch mehr geflossen und dicht als hakig, härter und fester als Gold, weicher und weniger fest als Kupfer. Hart gezogener Draht trägt auf 1 qmm Querschnitt 32–41 kg, geglüht 18–19,5 kg. Das S. ist höchst dehnbar und hämmerbar (Blattsilber), Atomgewicht 107,93, spezifisches Gewicht gegossen 10,424, gepreßt 10,566, destilliert 10,575, es schmilzt leichter als Gold und Kupfer, bei 962°, siedet bei 2050°, ist bei Weißglut flüchtig unter Bildung eines blauen Dampfes, absorbiert (wenn frei von Gold und Kupfer) beim Schmelzen an der Luft Sauerstoff, der beim Erstarren unter Spratzen entweicht, und zieht sich beim Erstarren stark zusammen. S. oxydiert sich nur im Sauerstoffgebläse und in sein verteiltem Zustand bei gewöhnlicher Temperatur durch Ozon. Es verbindet sich direkt mit Chlor, Brom und Jod, läuft durch Schwefel- und Phosphorwasserstoff an, schmilzt leicht mit Schwefel zusammen, wird von schmelzendem Ätzkali und Salpeter nicht angegriffen, bildet mit Schwefelleber Schwefelsilber und wird von schmelzendem Glas als Silikat aufgenommen und färbt es gelb. Es löst sich in konzentrierter Schwefelsäure unter Entwickelung von Schwefliger Säure und in mäßig konzentrierter Salpetersäure unter Entwickelung roter Dämpfe; von verdünnter Schwefelsäure und Salzsäure wird kompaktes S. nicht angegriffen; es gibt mit Chromsäure rotes chromsaures S. und wird durch viele Metalle und Reduktionsmittel, auch durch organische Substanzen (besonders Aldehyde) aus seinen Losungen gefällt (dendritisch aus Lösungen abgeschiedenes S. bildet den Silberbaum [Dianenbaum], der sich sehr schön beim Übergießen von Quecksilber mit einer Lösung von salpetersaurem S. ausbildet). S. ist einwertig; man kennt ein Oxydul Ag4O (?), ein Oxyd Ag2O und ein Superoxyd AgO. Die Lösungen wirken ätzend giftig, doch kommt nur das salpetersaure S. in Betracht. Man benutzt reines S. fast nur zu chemischen Geräten; im übrigen wird zu Münzen, Schmuckwaren etc. legiertes S. verarbeitet, und aus[463] diesem bereitet man auch zahlreiche Präparate für die Photographie und Medizin, zum Versilbern von Metall und Glas (Silberspiegel), zu Glas- und Porzellan farben etc. Molekulares S. benutzt man zur Synthese organischer Präparate, kolloidales S. findet arzneiliche Verwendung bei Entzündung der Lymphgefäße, Phlegmone, Bindehautentzündung, Magen-, Darm-, Nervenerkrankungen, auf Wunden etc., in der Veterinärpraxis bei Pferdetyphus und Katarrhalfieber des Rindes. Man rühmt ihm insektionshemmende Eigenschaften nach.
[Geschichtliches.] S. gehört zu den dem Menschen am frühesten bekannt gewordenen Metallen. Der Reichtum der Phöniker stammte aus dem spanischen Silberhandel, vor diesem aber gewannen sie S. in Kleinasien, Cypern, Thrakien, vielleicht auch in Afrika. Homer erwähnt S. häufiger und nennt Chalybien als Land seiner Herkunft. Die Silbergruben in Attika werden zuerst von Äschylos erwähnt, die Athener waren in Laurion jedenfalls Nachfolger asiatischer Völker. Dieser Bergbau lieferte zur Zeit des Themistokles über 2 Mill. Mk., hörte aber 102 v. Chr. auf. Alexander d. Gr. zog aus dem Silberbergwerk am See Prasias täglich 28 kg S. Bei den Römern blieb S. bis zu den Punischen Kriegen selten, der spätere große Silberreichtum Roms stammte wesentlich aus Spanien. Nach Polybios arbeiteten in den Bergwerken von Neukarthago 40,000 Menschen. Ungeheure Silbermengen waren in den Hauptstädten asi anscher Reiche aufgespeichert. Die alten Germanen besaßen wenig S., Tacitus kennt nur ein einziges Silberbergwerk in Deutschland (bei Wiesbaden oder Ems), das aber bald einging. Ein bedeutender Silberbergbau entstand später im Lebertal bei Markirch im Elsaß. Die Lagerstätten des Rammelsberges wurden seit 968 ausgebeutet, ein großer Teil des Silbers, das vom 10.–12. Jahrh. in Europa im Umlauf war, stammte aus dem Harz. Die Silbergewinnung von Andreasberg begann im Anfang des 15. Jahrh. In Sachsen soll der Bergbau bei Mittweida und Frankenburg 922–930 rege geworden sein, bei Freiberg begann er um 1163, bei Schneeberg 1471, bei Annaberg 1496. In Böhmen wurde schon im 8. Jahrh. auf S. gebaut; Kuttenberg gab 1240–1620 fast 2 Mill. kg S. Das sächsisch-böhmische Erzgebirge spielte Anfang des 16. Jahrh. dieselbe Rolle wie später Kalifornien. In Mähren soll der Bergbau von Iglau der älteste sein, im 11. Jahrh. waren die Gruben von Zeyring in Steiermark berühmt, Schladming wird schon im 13. Jahrh. genannt. In Schweden waren die Gruben von Sala schon im 8. Jahrh. in Betrieb, ihre blühendste Periode fällt in die erste Hälfte des 16. Jahrh.; Kongsberg in Norwegen wurde 1623 durch deutsche Bergleute eröffnet. Im Ural begann der Silberbergbau 1814, am Altai 1743, im Bezirk Nertschinsk 1704. In Spanien ging die seit dem Altertum berühmte Grube bei Guadalcanal in die Hände der Fugger über, die ungeheure Reichtümer aus derselben zogen, bis sich die Grube mit Wasser füllte und dann verlassen wurde. 1839 wurden die Gruben der Sierra Almagrera in der Provinz Almeria und 1843 die von Hiendelaencina in Guadalajara entdeckt, und seit Einführung des Pattinsonschen Prozesses gewinnt man viel S. aus den Bleierzen der Sierra de Gador und von Cartagena. Die großartigste Umgestaltung erfuhr die Silberproduktion durch die Entdeckung Amerikas, nachdem Cortez in Mexiko eingedrungen war; 1522 kam das erste S. aus Mexiko nach Europa, 30 oder 40 Jahre später waren dort die Gruben in vollem Gang, und auch Peru lieferte alsbald viel Gold und S., besonders seitdem 1545 die berühmten Gruben von Cerro de Potosi entdeckt worden waren. Die Silberproduktion verzehnfachte sich durch diese Entdeckungen. Erheblich gesteigert wurde die amerikanische Produktion durch Einführung des Amalgamationsprozesses, der 1557 von Bartholomäus de Medina entdeckt und seit 1566 im großen ausgeführt, 1571 in Bolivia und Peru eingeführt wurde. Im 17. Jahrh. wurden die Silberbergwerke zu Yauricocha oder Paseo im nördlichen Peru eröffnet und lieferten reiche Erträge. Als dann die Kämpfe begannen, die zur Trennung Perus von Spanien führten, sank die Silberproduktion und hob sich erst wieder in bedeutenderm Maß, als die Quecksilberfunde in Kalifornien die Ausbeutung erleichterten. Durch die Silberentdeckungen in den Vereinigten Staaten wurde aber schließlich alles Bisherige weit übertroffen. In Nevada, Utah, Colorado, Kalifornien, Arizona, Montana, Idaho, New Mexico, Oregon und Washington wurden reiche Erze entdeckt, und namentlich der Comstockgang bei Virginia City in Nevada lieferte seit 1859 enorme Mengen S. und Gold. Seit den 1870er Jahren hat die Silbergewinnung in den Vereinigten Staaten die von Mexiko überholt, und die Union ist jetzt der größte Silberproduzent. 1885 begann Neusüdwales S. zu liefern (Broken Hill Gruben), und in den letzten Jahren stand Australien als Silberproduzent an dritter Stelle. – Im Altertum wurde das S. durch Verbleien und Abtreiben gewonnen; diese Prozesse waren bis über die Mitte des 16. Jahrh. allein maßgebend und sind noch gegenwärtig von größter Bedeutung. Der Amalgamationsprozeß fand erst 1784 in Europa Anwendung. Um die Mitte des 19. Jahrh. wurden auf Kupferhüttenprodukte die Kochsalzlaugerei von Augustin, die Wasserlaugerei von Ziervogel, die Schwefelsäurelaugerei, die Hyposulfitlaugerei von Patera angewandt. In neuester Zeit spielt die elektrolytische Entsilberung des Kupfers eine große Rolle. Von noch größerer Tragweite ist für die Entsilberung des Werkbleies der 1833 erfundene Kristallisationsprozeß von Pattinson und der 1850 patentierte Zinkentsilberungsprozeß von Parkes, der durch Cordurié verbessert wurde. Die Produktion des Silbers im Altertum kann nicht geschätzt werden. Viele Berichte erzählen von gewaltigen Mengen, daß aber z. B. David zum Tempelbau 1 Mill. Ztr. S. gestiftet haben soll (Chronika 1,23,14) ist ganz gewiß übertrieben. Die Silberproduktion einzelner Länder ist seit 1493 bekannt. In den 28 Jahren von 1493–1520 produzierten Deutschland 308,000, Österreich-Ungarn 672,000, das übrige Europa 336,000, andre Länder 1400, die Welt 1,317,400, also im Jahr durchschnittlich 47,000 kg.
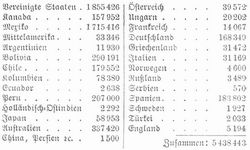
Die Silberproduktion im J. 1901 betrug in Kilogrammen in
[464] Die Silberproduktion der Welt betrug im Durchschnitt jährlich in Kilogrammen:
In Deutschland waren einst die Freiberger Gruben und der Oberharz die Hauptproduzenten. Daneben trat der Mansfelder Bezirk auf, der in den letzten Jahren jene überflügelte. Gegenwärtig erzeugen das meiste S. die Hütten im Rheinland, meist aus ausländischen Erzen. Die Produktion betrug in Kilogrammen:
Die Hauptproduzenten lieferten in Kilogrammen:
Der Verbrauch an S. zu technischen Zwecken wird für 1900 auf 1277 Ton. berechnet. Davon entfallen auf Nordamerika 356, England 225, Frankreich 197, Deutschland 150, Rußland 115, Österreich-Ungarn 55 T. Hierbei ist der deutsche Verbrauch zu niedrig angegeben. Vgl. Sueß, Die Zukunft des Silbers (Wien 1892); Bamberger, Silber (Berl. 1892); Stall, Die Zukunft des Silbers (das. 1893); Kröhnke, Methode zur Entsilberung von Erzen (Stuttg. 1900); B. Neumann, Die Metalle (Halle 1904), sowie die Literatur bei Artikel »Gold«, »Edelmetalle« und »Hüttenkunde«.
Adelung-1793: Silber-Service, das · Silber-Tinktur, die · Silber-Vitriol, der · Capellen-Silber, das · Silber, das · Silber-Page, der
Brockhaus-1911: Silber · Silber [2] · Galvanisiertes Silber · Oxydiertes Silber
Herder-1854: Silber · Seißi-Silber · Salpetersaures Silber
Lueger-1904: Silber [3] · Silber [4] · Silber, grünes · Photographische Silber-, Gold- und Platinrückstände · Silber [1] · Silber [2]
Meyers-1905: Silber, galvanisiertes, oxydiertes · Schwefelsaures Silber · Silber, güldisches · Silber, grünes · Salpetersaures Silber · Galvanisiertes Silber · Chromsaures Silber, saures · Oxydiertes Silber · Güldisches Silber
Pierer-1857: Silber [1] · Seißi Silber · Zehnlöthiges Silber · Silber [2] · Muschliges Silber · Geschlagenes Silber · German silber · Kupferiges Silber · Griechische Vergoldung auf Silber
Buchempfehlung
Schnitzler, Arthur
Traumnovelle
Die vordergründig glückliche Ehe von Albertine und Fridolin verbirgt die ungestillten erotischen Begierden der beiden Partner, die sich in nächtlichen Eskapaden entladen. Schnitzlers Ergriffenheit von der Triebnatur des Menschen begleitet ihn seit seiner frühen Bekanntschaft mit Sigmund Freud, dessen Lehre er in seinem Werk literarisch spiegelt. Die Traumnovelle wurde 1999 unter dem Titel »Eyes Wide Shut« von Stanley Kubrick verfilmt.
64 Seiten, 4.80 Euro
Im Buch blättern
Ansehen bei Amazon
Buchempfehlung
Romantische Geschichten III. Sieben Erzählungen
Romantik! Das ist auch aber eben nicht nur eine Epoche. Wenn wir heute etwas romantisch finden oder nennen, schwingt darin die Sehnsucht und die Leidenschaft der jungen Autoren, die seit dem Ausklang des 18. Jahrhundert ihre Gefühlswelt gegen die von der Aufklärung geforderte Vernunft verteidigt haben. So sind vor 200 Jahren wundervolle Erzählungen entstanden. Sie handeln von der Suche nach einer verlorengegangenen Welt des Wunderbaren, sind melancholisch oder mythisch oder märchenhaft, jedenfalls aber romantisch - damals wie heute. Nach den erfolgreichen beiden ersten Bänden hat Michael Holzinger sieben weitere Meistererzählungen der Romantik zu einen dritten Band zusammengefasst.
- Ludwig Tieck Peter Lebrecht
- Friedrich de la Motte Fouqué Undine
- Ludwig Achim von Arnim Isabella von Ägypten
- Clemens Brentano Geschichte vom braven Kasperl und dem schönen Annerl
- E. T. A. Hoffmann Das Fräulein von Scuderi
- Joseph von Eichendorff Aus dem Leben eines Taugenichts
- Wilhelm Hauff Phantasien im Bremer Ratskeller
456 Seiten, 16.80 Euro
Ansehen bei Amazon
- ZenoServer 4.030.014
- Nutzungsbedingungen
- Datenschutzerklärung
- Impressum